医学中心张明杰、刘伟研究团队关于CaM/TRP离子通道相互作用的分子机制研究发表在Structure杂志

瞬时受体电位(Transient receptor potential,TRP)离子通道超家族是一类广泛表达于动物体内的阳离子通道,参与视觉、触觉、痛觉、味觉、温度感知等多种多样的生命活动进程。果蝇TRP(Drosophila TRP,TRP)离子通道是历史上第一个被发现的瞬时受体电位离子通道,在果蝇复眼的光视觉转导通路中发挥重要作用。作为对钙离子(Calcium,Ca2+)具有高度选择性的阳离子通道,Ca2+反过来对TRP离子通道存在正向和负向两种反馈调控。然而,Ca2+调控TRP离子通道的分子机制仍不清楚。之前的研究发现:钙离子效应蛋白--钙调蛋白(Calmodulin, CaM)可以结合TRP离子通道的羧基末端序列[1]。因此,研究者推测:Ca2+可能通过其效应蛋白CaM对其通道活性进行调节[2, 3]。
在此科学假说的驱动下,深圳北京大学香港科技大学医学中心的张明杰、刘伟课题组对CaM与TRP离子通道的相互作用进行了深入的研究。他们的研究结果发现:在TRP离子通道的羧基末端上,存在两个间隔较远的CaM结合位点(Calmodulin binding site,CBS)。有趣的是,两个CBS并不结合两个CaM;而是由一个CaM的氨基端亚基(N-lobe)选择性结合CBS1的同时,利用其羧基端亚基(C-lobe)结合CBS2。通过生物化学与结构生物学等手段,本研究解析了上述特异性相互作用的生化与结构基础,并找到了影响TRP离子通道与CaM相互作用的关键氨基酸位点。令人意外的是,破坏TRP离子通道与CaM的相互作用,并不影响生理条件下TRP离子通道对光刺激的响应,提示Ca2+对TRP离子通道的正向反馈和负向反馈调控并非通过CaM进行,而很可能是通过其他蛋白或者是由Ca2+直接参与了TRP离子通道的调控。本研究结果为领域内的研究者进一步探索Ca2+对TRP离子通道进行正向和负向反馈调控的分子机制,提供了有价值的科学线索。
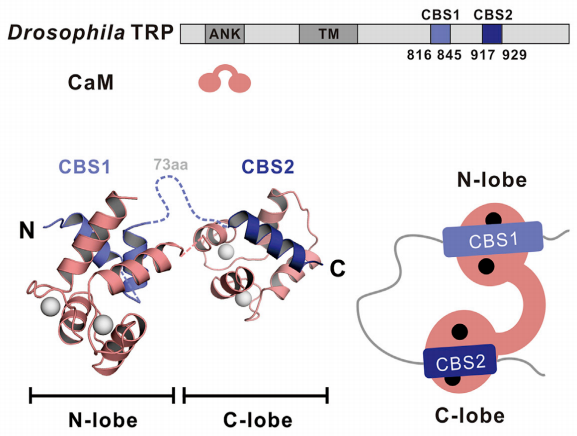
图1.研究结果概述
本研究通过生物化学与结构生物学手段,发现TRP离子通道羧基末端上存在两个可以与钙调蛋白结合的位点,CBS1(T802-K862)和CBS2(M899-D940)。有意思的是,完整的CBS12片段(T802-D940)却只能结合一个钙调蛋白。进一步的研究:CBS12与钙调蛋白之间存在一种意外的结合模式,即CBS1结合N-lobe,CBS2结合C-lobe。
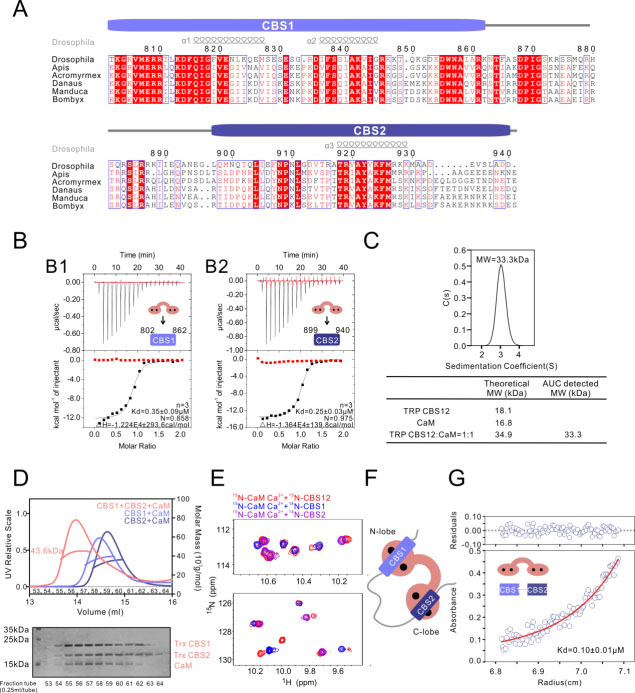
图2. CaM的N-lobe选择性结合TRP的CBS1,其C-lobe结合CBS2
通过分别解析CBS1/N-lobe蛋白复合物晶体结构和CBS2/C-lobe蛋白复合物晶体结构,本研究发现CBS1与N-lobe结合后会形成一种特殊的“螺旋-转折-螺旋”结构,而CBS2与C-lobe结合后则会形成经典的单次螺旋结构。通过突变CBS12上介导与钙调蛋白相互作用的关键氨基酸,可以完全打破CBS12片段与钙调蛋白的相互作用。
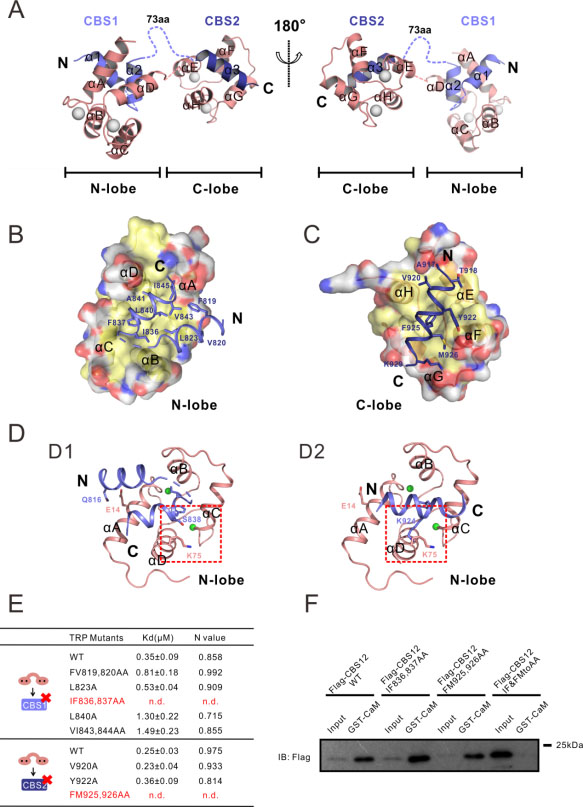
图3. N-lobe/CBS1 与C-lobe/CBS2复合物的晶体结构及其生化验证
再者,本研究发现,通过突变全长TRP离子通道上介导与钙调蛋白相互作用的关键氨基酸,可以完全打破内源性全长TRP离子通道与钙调蛋白的相互作用。令人意外的是,干扰TRP离子通道与钙调蛋白的结合却不影响生理条件下TRP离子通道对光刺激的响应。目前,TRP离子通道与钙调蛋白相互作用的生理功能还不是很清楚。
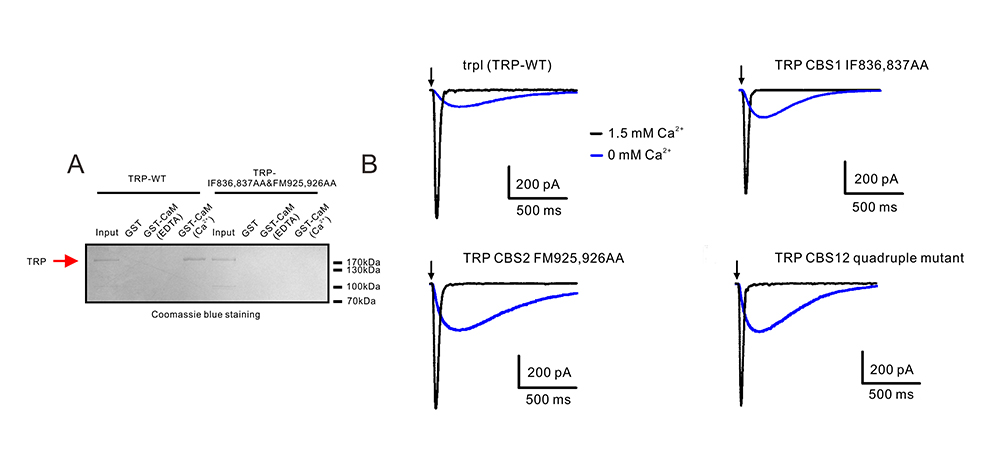
图4.CaM以钙离子依赖性的方式与纯化的全长TRP通道相互作用,破坏其相互作用位点未影响生理条件下TRP离子通道对光刺激的响应
最后,本研究发现,与果蝇TRP离子通道氨基酸序列最相近的哺乳类动物TRPC4离子通道,也存在类似的钙调蛋白结合模式。TRPC4离子通道CBS1与N-lobe结合后也会形成一种类似的“螺旋-转折-螺旋”结构。而钙调蛋白与TRP离子通道、TRPC4离子通道相互作用的生物学功能则有待进一步研究。

图5. TRPC4离子通道存在类似的钙调蛋白结合模式
参考文献:
1.Chevesich, J., A.J. Kreuz, and C. Montell, Requirement for the PDZ domain protein, INAD, for localization of the TRP store-operated channel to a signaling complex. Neuron, 1997. 18(1): p. 95-105.
2.Harteneck, C., Proteins modulating TRP channel function. Cell Calcium, 2003. 33(5-6): p. 303-10.
3.Zhu, M.X., Multiple roles of calmodulin and other Ca(2+)-binding proteins in the functional regulation of TRP channels. Pflugers Arch, 2005. 451(1): p. 105-15.
撰稿:陈伟荻 刘伟 修订:方征宇
打开链接下载阅读论文全文 https://authors.elsevier.com/a/1cFB83SNvbyV3-
